Antimikrobiyal Direnç Çözümü: Makrofajların Epigenetik Programlanması
Antimikrobiyal direnç (AMD), günümüzde küresel halk sağlığını tehdit eden en öncelikli majör krizlerden biri olarak tanımlanmaktadır. Nitekim Dünya Sağlık Örgütü (DSÖ), AMD'yi insanlığın karşı karşıya kaldığı ilk on kritik sağlık tehdidi arasında sınıflandırmıştır. Bu krizin derinleşmesindeki temel etyolojik faktör, mevcut antimikrobiyal ve antiviral farmakoterapötiklerin neredeyse tamamının spesifik ve dar spektrumlu hedeflere (hücre duvarı biyosentezi, protein translasyonu, nükleik asit replikasyonu veya spesifik enzimatik inhibisyon) yönelik etki mekanizmalarına dayanmasıdır. Patojenler, yüksek mutasyon frekansları ve horizontal gen transferi kapasiteleri sayesinde bu spesifik moleküler hedefleri hızla modifiye ederek konvansiyonel ajanları inaktif kılmaktadır. Farmasötik araştırma-geliştirme süreçlerinin, mikroorganizmaların bu evrimsel adaptasyon hızının gerisinde kalması sonucunda, yeni nesil antimikrobiyal ajanlara karşı dahi kısa sürede dirençli suşlar gelişmektedir. Benzer biçimde, yüksek mutasyon ve replikasyon kinetiğine sahip RNA virüsleri karşısında da mevcut antiviraller yapısal kısıtlılıkları nedeniyle klinik etkinliklerini hızla yitirmektedir.
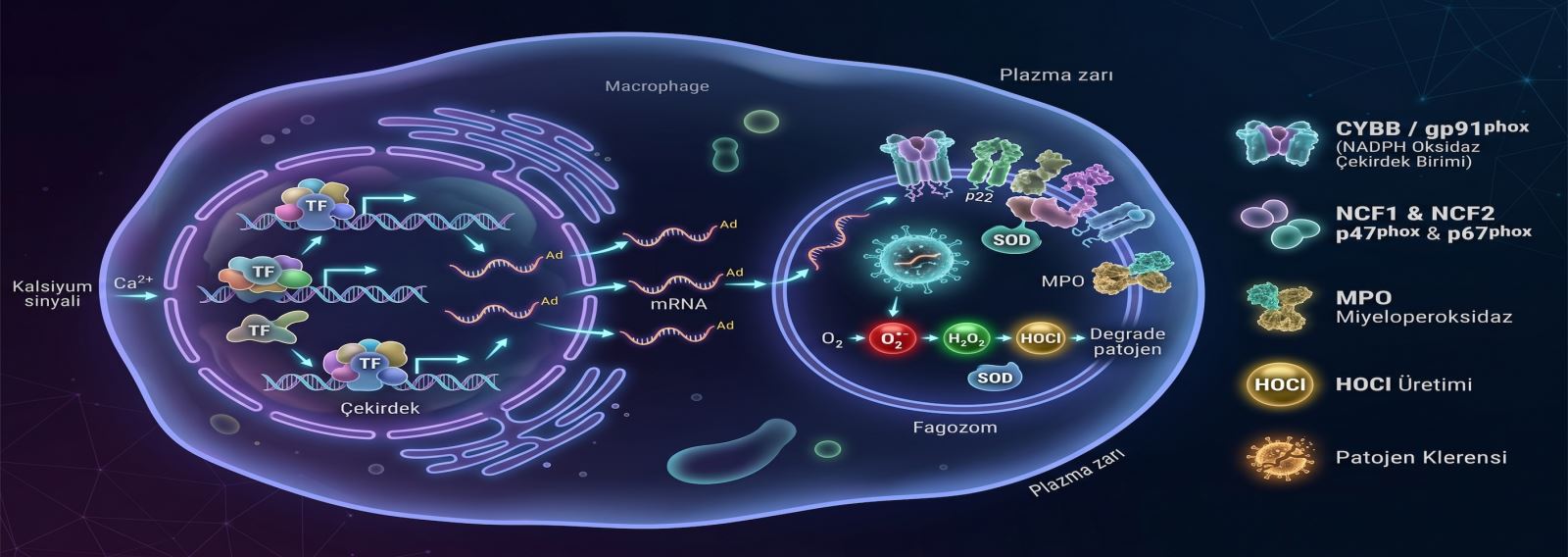
Doğal İmmün Yanıtın Yeniden Keşfi: Makrofajların Epigenetik Reprogramlanması Mevcut farmakolojik darboğazın aşılmasında, evrimsel süreçte yüksek düzeyde korunmuş ve direnç gelişimine tolerans tanımayan hücresel savunma mekanizmaları—özellikle makrofaj aracılı doğal immün yanıt—köklü bir çözüm sunmaktadır. Bazal fagositik işlevlere sahip makrofajlar, epigenetik olarak modüle edildiklerinde (yeniden programlandıklarında), pasif temizleyici hücre fenotipinden çıkarak hedefe yönelik, mikrobisidal kapasitesi maksimize edilmiş primer efektör hücrelere dönüşmektedir. Bu epigenetik transformasyon; patojen inaktivasyonunda merkezi rol oynayan NADPH oksidaz kompleksinin katalitik alt birimini kodlayan CYBB (gp91phox) ve doğrudan hipokloröz asit sentezinden sorumlu olan miyeloperoksidaz (MPO) genlerinin güçlü bir transkripsiyonel aktivasyonunu tetikler.
Solunum Patlaması ve Endojen HOCl Biyosentezi Söz konusu genetik uyarım, makrofajın fagolizozom lümeninde hücresel düzeyde "solunum patlaması" (respiratory burst) olarak adlandırılan şiddetli bir oksidatif kaskadı başlatır. Fagositoz yoluyla internalize edilen patojen, vezikül içerisinde öncelikle süperoksit radikallerine ve akabinde hidrojen peroksit (H₂O₂) maruziyetine uğrar. Kaskadın terminal aşamasında devreye giren MPO enzimi, H₂O₂ ile hücresel ortamdaki fizyolojik klorür (Cl⁻) iyonlarını katalitik bir reaksiyona sokarak, memeli immün sisteminin en potent endojen biyosidal ajanlarından biri olan hipokloröz asidi (HOCl) sentezler. İn vitro inorganik dezenfektanların aktif bileşenine biyokimyasal olarak benzeyen ancak organizma tarafından sıkı kontrollü hücresel mikrodosajlarda üretilen bu molekül, eşsiz bir patosidal silahtır.
Endojen HOCl, fagosite edilen patojene karşı akut ve agresif bir fizikokimyasal reaksiyon sergiler; viral protein kapsidlerini okside ederek denatüre eder, lipid kılıf bütünlüğünü bozar ve nükleik asit (DNA/RNA) zincirlerinde geri dönüşümsüz degradasyona yol açar. Bu mekanizma, patojenin saniyeler içerisinde nötralize edilmesini sağlayarak hızlı ve sterilizan bir doğal hücresel klerens (temizlenme) sağlar.
Adaptif İmmünitenin Stratejik Orkestrasyonu Makrofajların immünolojik fonksiyonu salt akut patojen eliminasyonu ile sınırlı kalmayıp, adaptif immün yanıtın orkestrasyonunda kritik bir evreye geçer. Hücresel yıkım sonucu açığa çıkan immünojenik viral veya bakteriyel protein fragmanları (antijenler), makrofajın "profesyonel antijen sunan hücre" (APC) kimliğiyle Majör Histokompatibilite Kompleksi (MHC) Sınıf I ve II molekülleri üzerinden hücre yüzeyinde eksprese edilir. Drene edici lenf nodlarına migrasyonu takiben bu antijenler naif T lenfositlerine sunulur. Bu spesifik interaksiyon, CD4+ yardımcı T hücrelerini aktive ederek B lenfositleri üzerinden patojene özgü yüksek afiniteli nötralizan antikorların klonlanmasını ve sekresyonunu uyarır. Eş zamanlı olarak aktive olan CD8+ sitotoksik T hücreleri ise, enfekte olmuş konak hücrelerini hedef alarak sistemli apoptozu indükler. Bu ardışık bilgi aktarımı kaskadı, olası sekonder maruziyetlere karşı immünolojik hafıza aracılığıyla çok daha hızlı ve şiddetli bir yanıt oluşturulmasını güvence altına alarak kalıcı adaptif bağışıklığı tesis eder.
Direnç Gelişiminin Biyofiziksel ve İstatistiksel İmkânsızlığı Bu mekanizmanın konvansiyonel terapötiklere kıyasla en devrimsel niteliği, HOCl’ün patojen üzerinde yarattığı pleiotropik oksidatif hasardır. Geleneksel moleküller spesifik bir enzimatik yolağı inhibe ederken; HOCl, mikrobiyal yapının temel biyokimyasal yapıtaşlarını (proteinlerdeki sülfhidril gruplarını, membran lipid çift tabakalarını ve nükleotit bazlarını) doğrudan, eş zamanlı ve spesifik olmayan bir biçimde okside eder. Bu geniş spektrumlu destrüksiyon modeli, patojenin mutasyonel bir immün kaçış geliştiremeyeceği kadar temel bir hücresel hasardır ve mikroorganizmaların HOCl’e karşı direnç geliştirmesini biyolojik açıdan neredeyse imkânsız kılar.
Konvansiyonel antibiyotiklere karşı tekil bir nokta mutasyonu hücresel direnç için yeterli olabilirken; bir patojenin HOCl'e direnç geliştirebilmesi için hücresel canlılığını bozmadan çok sayıda bağımsız mutasyonu aynı hücre soyunda eş zamanlı olarak biriktirmesi elzemdir. Bir bakteride; membran lipid konfigürasyonu, elektron transport zinciri enzimleri, DNA onarım mekanizmaları ve hücresel redoks dengesinden sorumlu genetik lokusların tamamının yaşamsal fonksiyonları koruyarak aynı anda mutasyona uğraması zorunluluğu, kümülatif adaptasyon olasılığını basit bir çarpımsal olasılıkla (örn. en az beş bağımsız lokus için ~10⁻³⁵) istatistiksel bir imkânsızlık düzeyine çeker. Zarflı virüslerde; lipid çift katmanının, yüzey glikoproteinlerinin ve nükleokapsid sistein rezidülerinin eş zamanlı yapısal değişimi viral enfektivite ile kesinlikle bağdaşmaz. Zarfsız virüslerde ise, kapsid yapısındaki tüm oksitlenebilir amino asitlerin eş zamanlı konformasyonel değişimi, kapsid geometrisini ve viral paketleme verimini bozacağından patojenin yaşam döngüsünü imkânsız hâle getirir. Dolayısıyla HOCl'ün çok hedefli yıkım kapasitesi, direnç gelişimi için ihtiyaç duyulan evrimsel sıçramayı biyo-matematiksel olasılık sınırlarının tamamen ötesine taşımaktadır.
Klinik Translasyon ve Sonuç Sonuç olarak; epigenetik olarak yeniden programlanmış makrofajların artırılmış ve kontrollü hücresel HOCl üretim kapasitesi, viral, bakteriyel ve fungal patojenleri direnç riski barındırmaksızın eradike ederek antimikrobiyal direnç sorununun moleküler kökenine inmektedir. Vücudun endojen immün potansiyelini maksimize eden bu hücresel aktivasyon stratejisi, patojen türünden bağımsız, pan-mikrobiyal ve geniş spektrumlu bir savunma avantajı sunmaktadır.
Geliştirdiğimiz Biyomimetik Biyoelektriksel Modülasyon metodolojisi aracılığıyla makrofajlarda indüklenen bu epigenetik yeniden programlanma, hücresel aktivasyon ve patojen eliminasyon kaskadı; in vivo hayvan modellerinde ve klinik insan çalışmalarında hücresel düzeyde bilimsel olarak valide edilmiştir. Makrofajların bu şekilde modüle edilmesi, mevcut AMD krizinin aşılmasının yanı sıra gelecekteki viral pandemilerin ve majör halk sağlığı tehditlerinin profilaktik ve terapötik yönetiminde kritik bir paradigma değişimi vadetmektedir.